撰文/一般內科部 消化肝膽科 潘俊傑醫師
胃癌是全球常見的消化道惡性腫瘤之一,當癌細胞突破胃壁擴散至腹膜或其他遠端器官時,傳統上常被視為「末期(第四期)胃癌」──治療選項少、預後不佳。然而,在2025年全球頂尖胃癌學術盛會之一的第16屆國際胃癌大會(IGCC) 上,專家們聚焦討論了一個正在改變臨床思維的重要議題:有限期第四期胃癌(limited stage IV gastric cancer)可能擁有新的治療策略與希望。
一般而言,第四期胃癌是指癌細胞已由原發腫瘤擴散至身體其他部位,如腹膜、肝臟或肺部等。其中,腹膜轉移是最常見、同時也是治療上最具挑戰性的類型之一。
當癌細胞播散至腹膜後,由於腹膜與血管之間存在一道天然的生理屏障,使得傳統的靜脈化學治療藥物難以在腹腔內達到足夠的有效濃度,導致系統性化療的治療效果受到明顯限制。這正是第四期胃癌病人整體治療困難、中位存活期普遍偏短的重要原因之一。
然而,臨床上有些病人的轉移範圍相對較小、局限性較強,例如主要位於腹膜,並沒有廣泛器官轉移,專家稱這類病人為 「有限期第四期胃癌」。未來這類病人有機會透過新的治療方式,延長存活時間和提高生活品質。
治療有限期第四期胃癌的新策略
目前,有限期第四期胃癌的治療仍以全身化療為主,但隨著醫學不斷進步,越來越多創新策略正陸續進入臨床研究階段,為包含腹膜轉移的有限期第四期胃癌病人帶來新的治療希望:
★新策略1:腹腔內化療(Intraperitoneal Chemotherapy, IP)
根據於2025年ASCO胃腸道癌症研討會(ASCO Gastrointestinal Cancers Symposium)發表的數據¹,在標準的靜脈注射(IV)紫杉醇合併 S-1(口服氟嘧啶類衍生物)治療中加入腹腔內(IP)紫杉醇,可顯著延長胃癌腹膜轉移病人的整體存活期。
DRAGON-01試驗提供了目前證據力最高的臨床數據。該研究為一項多中心、隨機、第三期臨床試驗,納入確診為胃癌並合併腹膜轉移的病人,比較在標準治療(靜脈注射紫杉醇合併口服 S-1)中,是否加入腹腔內紫杉醇可帶來額外的存活效益。
試驗結果顯示,接受腹腔內紫杉醇合併治療的病人,中位整體存活期達19.4個月,顯著優於僅接受標準治療組的13.9個月,死亡風險降低約34%(HR約0.66)。這是首次由大型隨機對照試驗明確證實,在胃癌腹膜轉移的治療中加入腹腔內化療,能帶來具統計與臨床意義的整體存活期延長。然而,2018年發表於Journal of Clinical Oncology的PHOENIX-GC試驗,則呈現了不同的研究結果2。該研究為日本多中心主導的第三期隨機臨床試驗,納入已確診腹膜轉移之胃癌病人,比較腹腔內合併靜脈注射紫杉醇加S-1與標準全身性化療(S-1加順鉑)在整體存活期上的差異。
結果顯示,雖然腹腔內治療組的中位整體存活期(17.7個月)較對照組(15.2個月)有延長趨勢,但該差異未達統計學顯著性(HR約0.72,p=0.080),因此未能證實腹腔內化療可明確改善整體存活期。
造成兩者結果差異的原因,可能與研究設計、對照治療方案、病人基線特徵等多項因素有關。目前在台灣雖然已有部分醫學中心嘗試作為整合性治療策略之一,但需要注意的是,腹腔內化療尚未被納入現行醫療指引所建議的第四期胃癌標準治療流程,因此其適應性與執行時機,仍須由具相關專業經驗的醫師依個別病人的臨床狀況審慎評估後決定。
整體而言,專家普遍認為此治療策略仍需進行更多的臨床試驗,以釐清最佳藥物組合、治療時機與適合族群,方能確立其在臨床實務中的精準定位。
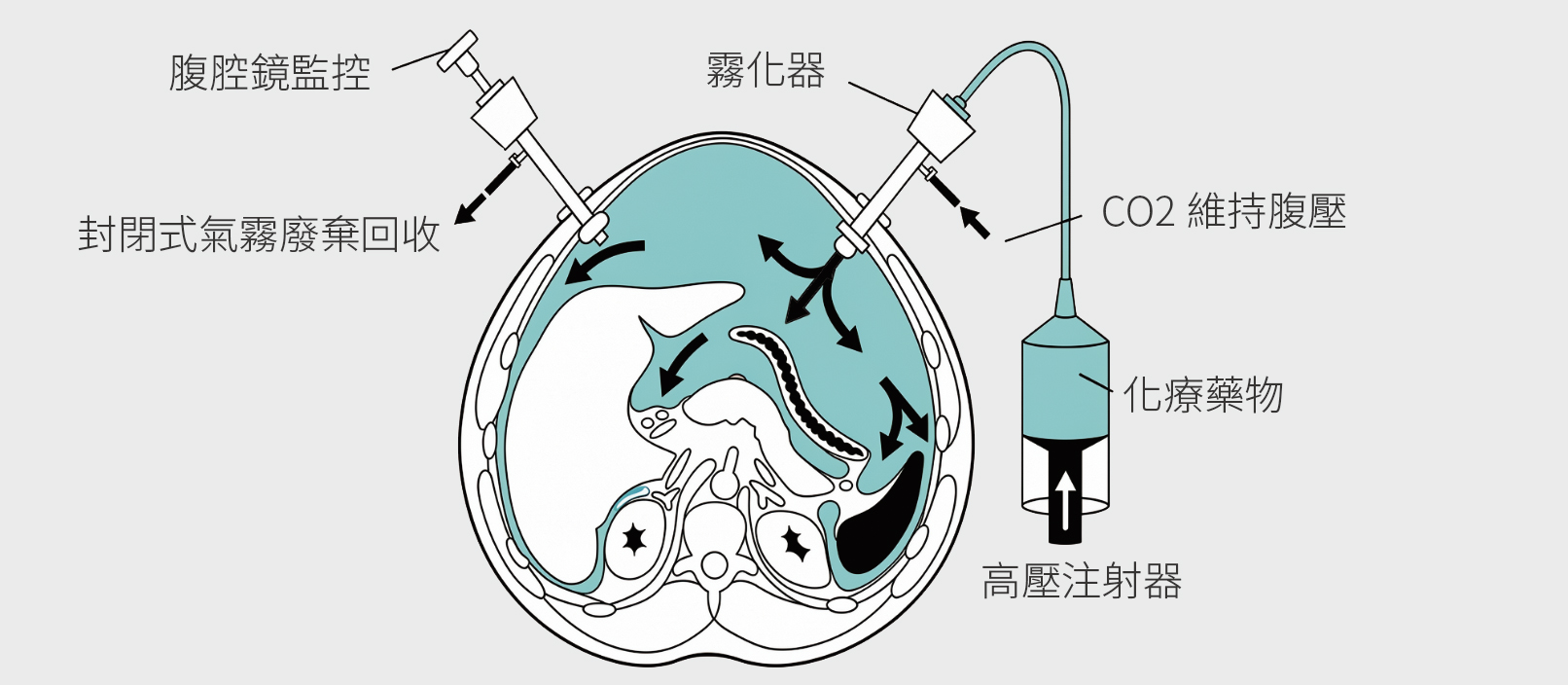
★新策略2:加壓式腹腔內氣霧化化療(PIPAC)
PIPAC(Pressurized Intraperitoneal Aerosol Chemotherapy)是一種微創治療方式,透過腹腔鏡將化療藥物轉換為細小氣霧顆粒,並在密閉加壓的腹腔環境中噴灑,使藥物均勻分布於腹膜表面,並提高對腫瘤的滲透深度。與傳統靜脈或腹腔灌注化療相比,PIPAC可改善藥物在腹膜的分布與吸收,同時降低全身毒性。
PIPAC的優勢包括:使用較低劑量即可達到局部治療效果;對骨髓、腎臟及神經系統影響較小;可重複施作,通常每6~8週進行一次;微創手術後恢復快、耐受性佳,特別適合腹膜轉移限制其他治療選項的病人。
此外,根據2025年6月發表於Gastroenterology Report 的一篇系統性回顧與統合分析3,研究團隊整理了18篇研究、671名病人,合計1,357次 PIPAC程序。結果顯示約三分之一病人完成至少三次治療,中位整體存活期約11.7個月,部分病人在組織學評估中亦顯示腫瘤產生了可測量或可觀察的變化。不良事件發生率約17%,其中僅3.6%為嚴重事件,治療相關死亡率極低(約 0.1%)。
研究團隊指出,PIPAC為晚期胃癌腹膜轉移病人提供了一種新的治療選擇,但目前大多數研究仍屬回顧性或小型前瞻性研究,在台灣目前也只有少數幾例實驗性治療個案,未來仍需更大規模、隨機對照試驗來確立其臨床效果與最佳治療策略。
★新策略 3:轉化治療(Conversion Therapy)
隨著腹腔內化療以及PIPAC技術的發展,一種稱為轉化治療的新策略,也逐步成形。所謂轉化治療,是指先透過腹腔內化療或PIPAC顯著降低腫瘤負荷,再評估病人是否有機會接受手術。換言之,原本被認為不可切除的腹膜轉移病人,在這種策略下,可能轉變為可手術狀態。
2024年5月發表於 British Journal of Surgery的系統性回顧與統合分析4,發現接受腹腔內化療後約16%的病人成功進入轉化手術階段,顯示腹膜病灶有可能可縮小至可手術的程度。然而,轉化治療並非適合所有病人,需由外科、腫瘤科、放射科等多科團隊共同評估,挑選出最適合接受手術的病人,確保治療安全性與療效。
從「末期」走向「新可能」
在第16屆國際胃癌大會的討論中,專家一致強調:胃癌第四期不再是僅能緩和治療,而是開始思考更多可能性。透過新興的多重治療策略,部分病人可以得到更好的控制。雖然這些療法仍處於臨床試驗或初期實踐階段,但它們代表了「為困難局面尋找突破」的醫療精神。未來,隨著更多研究數據的累積,有限期的第四期胃癌的治療藍圖也將更加清晰。
胃癌如何分期?
胃癌分期是以腫瘤侵犯胃壁深度、淋巴結轉移數目與有無遠端轉移來決定。胃癌第四期是指腫瘤已侵犯胃壁、有7個以上淋巴轉移、無遠端轉移;或腫瘤已侵犯胃壁、有淋巴轉移、有遠端轉移
參考資料
- DRAGON-01 Trial – Intraperitoneal paclitaxel combination improves overall survival in gastric cancer with peritoneal metastases. ASCO / The ASCO Post, 2025 Mar 25. Available from: https://ascopost.com/issues/march-25-2025/intraperitoneal-paclitaxel-combination-regimen-improves-overall-survival-in-advanced-gastric-cancer
- Ishigami, H., Fujiwara, Y., Fukushima, R., Nashimoto, A., Yabusaki, H., Imano, M., Imamoto, H., Kodera, Y., Uenosono, Y., Amagai, K., Kadowaki, S., Miwa, H., Yamaguchi, H., Yamaguchi, T., Miyaji, T., & Kitayama, J. (2018). Phase III trial comparing intraperitoneal and intravenous paclitaxel plus S‑1 versus cisplatin plus S‑1 in patients with gastric cancer with peritoneal metastasis: PHOENIX‑GC trial. Journal of Clinical Oncology, 36(19), 1922–1929. https://doi.org/10.1200/JCO.2018.77.8613
- Lee, J. H., Choi, Y. Y., Kim, J. W., et al. (2021). Pressurized intraperitoneal aerosol chemotherapy (PIPAC) for gastric cancer with peritoneal metastasis: Current status and perspectives. Gastroenterology Report, 9, 1–12. https://doi.org/10.1093/gastro/goaf040
- Guchelaar, N. A. D., Nasserinejad, K., Mostert, B., et al. (2024). Intraperitoneal chemotherapy for peritoneal metastases of gastric origin: A systematic review and meta-analysis. British Journal of Surgery, 111(5), znae116. https://doi.org/10.1093/bjs/znae116








